NO ME SALEN
(APUNTES TEÓRICOS Y EJERCICIOS DE BIOFÍSICA DEL CBC)
CALOR Y TERMODINÁMICA
|
|

|
 |
 |
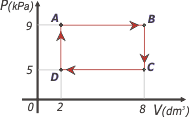
Ad. 28* - Un mol de gas ideal monoatómico realiza el ciclo ABCDA reversible como se indica en la figura:
a) Calcular el calor intercambiado en la evolución ABC indicando si es cedido o absorbido por el sistema.
(cp = 5R/2; cv = 3R/2)
|
 |
|
|
| |
Es un ejercicio sencillo, pero con varias "trampitas". Prestá atención.
Como en casi todos los ejercicios de evoluciones gaseosas suelo hacer un cuadro para ir volcando la información, ya que permite comprender fácilmente los pasos que vamos realizando y chequear que los números van cerrando. |
|
|
Y lo primero que hacemos es llenar los casilleros sencillos, inmediatos: aquellos que valen cero.
En las evoluciones isocóricas el trabajo es nulo (no hay área encerrada bajo la curva). ya van dos ceros.
La variación de energía interna de todo ciclo cerrado (perdón por la redundancia) también es nula, porque siendo la energía interna una función de estado, y partiendo y llegando al mismo estado... |
| (J) |
Q |
ΔU |
W |
| AB |
|
|
|
| BC |
|
|
0 |
| CD |
|
|
|
| DA |
|
|
0 |
| ciclo |
|
0 |
|
|
|
|
|
Vamos a calcular el resto de los trabajos. Pero antes dejame hacerte una aclaración. La unidad de volumen utilizada es el decímetro cúbico (que es lo mismo que un litro) y es la milésima parte del metro cúbico, 1 dm3 = 10-3 m3. Por otro lado las presiones vienen expresadas en kPa, o sea 103 Pa. De modo que el producto entre kPa . dm3 es lo mismo que 103 Pa . 10-3 m3 = Pa . m3 = J (joules). Habrás visto que la unidad que consigné en el cuadro es, justamente, J. |
|
10n.10-n = 1
103.10-3 = 1 |
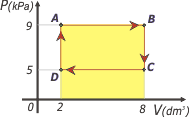 |
El trabajo en la transformación AB (una isobárica) podés calcularlo como:
WAB = PAB . ΔVAB
WAB = 9 x 103 Pa . 6 x 10-3 m3
WAB = 54 J
|
|
|
en un gráfico p/v el área encerrada bajo la curva representa al trabajo entre dos estados |
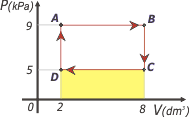
| El trabajo del gas en la transformación CD es otra isobárica, se calcula de la misma manera que la anterior: |
|
|
|
WCD = PCD . ΔVCD
WCD = 5 x 103 Pa . (– 6 x 10-3 m3)
WCA = – 30 J
Se trata de un trabajo negativo ya que se corresponde con una reducción de volumen. |
|
|
|
El trabajo del gas durante el ciclo es la suma de los trabajos parciales. De modo que ya tenemos otra respuesta:
Wciclo = 24 J
Fijate que esos 24 J están representados, justamente por el área encerrada dentro del ciclo (6 x 4 = 24). |
|
|
Dentro de cada renglón también hay una lógica, que está dada por:
Q = ΔU + W
el primer principio de la termodinámica; de modo que el calor intercambiado durante el ciclo debe valer lo mismo que el trabajo, ya que la variación de energía vale cero. |
| (J) |
Q |
ΔU |
W |
| AB |
|
|
54 |
| BC |
|
|
0 |
| CD |
|
|
-30 |
| DA |
|
|
0 |
| ciclo |
24 |
0 |
24 |
|
|
|
|
Hasta acá fue demasiado sencillo. Lo que viene no es tan difícil. La cantidad de calor intercambiada en el tramo AB sale de:
QAB = cp n ΔTAB
Nos enfrentamos con que no conocemos ni el número de moles del gas ni las temperaturas. ¡Pero no desesperéis! Fijaos... como hacemos decenas de veces en las que operamos con gases ideales... utilizamos la ecuación de estado:
PA . VA = n R TA
PB . VB = n R TB
Si restamos miembro a miembro esas dos ecuaciones, nos queda:
PB . VB – PA . VA = n R TB – n R TA
En el primer miembro podemos sacar la presión como factor común, ya que PB = PA (que ahora llamaré PAB). Y en el segundo miembro saco n R como factor común.
PAB . ΔVAB = n R ΔTAB
De modo que el la fórmula del calor, en lugar de escribir n ΔTAB, podemos escribir
PAB . ΔVAB / R. Y recordando que cp vale 2,5 R, nos queda:
QAB = 2,5 PAB . ΔVAB
QAB = 2,5 . 9 x 103 Pa . 6 x 10-3 m3
QAB = 135 J
De la misma manera calculamos QCD.
QCD= 2,5 . 5 x 103 Pa . (– 6 x 10-3 m3)
QCD = – 75 J
|
|
la mayor parte de los estudiantes examinados no supo resolver este asunto: no contar con el número de moles ni las temperaturas.
Varios lograron salir del apuro inventando un valor arbitrario para el número de moles. Aunque los correctores lo aceptaron como válido es técnicamente incorrecto. |
|
Volquemos estos valores a la tabla porque se nos van a mezclar entre tantos números. Ya está.
Ahora vamos a calcular los calores intercambiados en las evoluciones isocóricas.
QBC = cv n ΔTBC
|
| (J) |
Q |
ΔU |
W |
| AB |
135 |
|
54 |
| BC |
|
|
0 |
| CD |
-75 |
|
-30 |
| DA |
|
|
0 |
| ciclo |
24 |
0 |
24 |
|
|
|
calor negativo significa que el gas lo cede
trabajo negativo significa que el gas lo recibe |
|
Estamos en el mismo problema de antes, no tenemos ni las temperaturas ni el número de moles... Pero ahora ya estamos cancheros y lo resolvemos de la misma manera, con la ayuda de la ecuación de estado. Ojo, fijate que lo que varía en este caso es la presión, mientras que lo que se mantiene constante es el volumen.
Resulta así:
QBC = 1,5 . ΔPBC . VBC
QBC = 1,5 . (– 4 x 103 Pa) . 8 x 10-3 m3
QBC = – 48 J
|
|
|
Y de la misma manera operamos para el tramo DA.
QDA = 12 J
Metamos todo en el cuadro antes de que se nos entrevere (jiji... qué palabra más antigua... entrevere). |
| (J) |
Q |
ΔU |
W |
| AB |
135 |
|
54 |
| BC |
-48 |
|
0 |
| CD |
-75 |
|
-30 |
| DA |
12 |
|
0 |
| ciclo |
24 |
0 |
24 |
|
|
|
|
Qué útil es la tabla, además de cuidar nuestro trabajo nos permite verificar que las cosas nos están dando bien. Mirá toda la columna: 135 – 48 – 75 + 12 = 24. ¿No es cierto?
Y ya tenemos las respuestas que solicita el enunciado, ya que el calor intercambiado en la evolución ABC es igual a la suma de los calores intercambiados en AB y BC.
QABC = QAB + QBC =
QABC = 135 J + (– 48 J) =
|
|
|
| |
QABC = 87 J Qciclo = 24 J |
|
|
|
|
| Los signos positivos de ambas respuestas nos indican que tanto en la evolución ABC como en el ciclo completo, el sistema recibe calor. |
|
|
Ya que estamos completamos todo el cuadro. Podemos hacerlo utilizando el primer principio (sumas horizontales), o aplicando las fórmulas de cálculo de variación de energía interna. Te lo dejo a vos.
Este ejercicio puede resolverse con mucho menos esfuerzo, calculando solamente lo que el enunciado pide. No me salen lo resuelve íntegramente para aprovechar la movida. |
| (J) |
Q |
ΔU |
W |
| AB |
135 |
81 |
54 |
| BC |
-48 |
-48 |
0 |
| CD |
-75 |
-45 |
-30 |
| DA |
12 |
12 |
0 |
| ciclo |
24 |
0 |
24 |
|
|
|
|
Tenés otros ejercicios muy parecidos aquí y acá. |
|
|
| |
 |
| *Este ejercicio fue parte del examen 2do. parcial, tomado el 23-nov-12. en varias sedes del CBC, Universidad de Buenos Aires. |
|
|
| Desafío: ¿Cuánto valdrá la variación de entropía para todo el ciclo? |
|
| |
|
| Algunos derechos reservados.
Se permite su reproducción citando la fuente. Última actualización nov-12. Buenos Aires, Argentina. |
|
|
| | |
|

