 |
NO ME SALEN
(APUNTES TEÓRICOS DE BIOFÍSICA DEL CBC)
EVOLUCIONES REVERSIBLES DE GASES IDEALES
|
|

W o L
son símbolos alternativos para
trabajo |
|
| |
Evoluciones reversibles de gases ideales
Una evolución de un gas entre dos estados diferentes (diferente volumen, diferente presión y diferente temperatura) suele representarse en gráficos presión-volumen como los de acá abajo. No hay restricciones para las evoluciones de verdad, y generalmente son tan caóticas que intentar una representación gráfica de una evolución real es utópico.
Sin embargo una evolución enormemente lenta y ordenada permitiría conocer en cada instante todas las variables termodinámicas del gas. A eso se lo llama evolución reversible y se caracteriza por tener definidos todos los estados intermedios entre dos cualesquiera.
El conocimiento que estas evoluciones ideales arrojan es muy valedero y permite establecer límites precisos a las transformaciones reales que ocurren en el universo. Muchas veces también ocurre, que resultan aproximaciones útiles para efectuar cálculos e inferencias. Por eso las estudiamos.
En esta tabla volqué las evoluciones más características, acompañadas de las fórmulas para calcular la energía implicada en el primer principio de la termodinámica,
Q = ΔU + W
|
| |
|
|
|
|
|
|
|
| |
isobárica |
isocórica |
isotérmica |
adiabática |
ciclo |
cualquiera |
| Q |
cp n ΔT |
cv n ΔT |
|
0 |
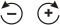 |
|
| ΔU |
cv n ΔT |
cv n ΔT |
0 |
cv n ΔT |
0 |
cv n ΔT |
| W |
p ΔV |
0 |
|
– cv n ΔT |
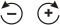 |
|
Donde cV y cP, son el calor específico molar a volumen constante
y el calor específico molar a presión constante, respectivamente;
para gases ideales monoatómicos cV = 1,5 R y cP = 2,5 R,
y para diatómicos cV = 2,5 R y cP = 3,5 R,
y donde R es la
constante universal de los gases ideales:
R = 8,314 J/mol K = 0,08207 l atm/mol K = 1,987207 cal/K mol |
|
Sin muchos detalles, los lineamientos básicos son:
- el calor, Q, se calcula con el mismo criterio que en calorimetría.
- el trabajo, W, se calcula realizando la operación integral: W = ∫ p dV; de ahí surge:
n R T ln (VF /V0).
- la energía interna de un gas, ΔU, depende (básicamente) de la temperatura, y además es una función de estado (dos apuntes más adelante me meto de lleno en este asunto). En el caso de un gas ideal, la energía interna depende exclusivamente de la temperatura.
- Siempre hay que tener a mano la ecuación de estado de los gases ideales,
P V = n R T, que puede sacarte de más de un apuro. Por ejemplo...
en una evolución isobárica, cp n ΔT = cp P ΔV / R
en una evolución isocórica, cv n ΔT = cv V ΔP / R
|
|
|
|
|
|
| CHISMES IMPORTANTES |
|
|
- Cuando Wilhelm Ostwald (1853-1932), premio Nobel de Química en 1909, introdujo el término mol en 1900, lo definió con base en una masa
proporcional a las masas relativas de las entidades elementales de las sustancias, lo
cual trajo el consabido problema de la interpretación del mol como una unidad de
masa.
Más tarde, con los avances en la teoría
atómico-molecular, un mol fue identificado como un número fijo de átomos,
moléculas, iones, etcétera, es decir, el número de Avogrado de entidades elementales.
Queda claro, entonces, que el mol nació para establecer cantidades de entidades cualesquiera.
- El aire es una mezcla de gases fundamental y mayoritariamente diatómicos, y se comporta casi como un gas ideal.
|
|
|
 |
| PREGUNTAS CAPCIOSAS |
|
|
- ¿Qué volumen ocupará un mol de un gas ideal a una atmósfera de presión y a 0°C de temperatura?
- Se dice que una evolución reversible o definida debe transcurrir lentamente... ¿pero qué es lentamente? ¿Más lento que qué?
|
|
|
| |
|
|
NOTA: No uses el cuadro de esta página como machete... trae mala suerte. Hace unos años le armé el machete a un estudiante y se sacó 1 (uno). En el curso siguiente se lo prestó a un compañero y se sacó 0 (cero). Se dio cuenta que la yeta estaba en este cuadro que usaba de machete y lo tiró por la ventana. El chofer de un colectivo se distrajo al ver el bollito cayendo y se estrelló contra un semáforo: 3 muertos y 15 heridos. ¡No lo uses!
Si invertís dos horas confeccionando tu propio machete vas a entender y aprender un montón de cosas que a la hora del examen son más útiles que esta hoja. |
|
|
 |
| |
| |
|
|
| Algunos derechos reservados.
Se permite su reproducción citando la fuente. Última actualización nov-07. Buenos Aires, Argentina. |
|
|
 |
| | |
|
|

