NO ME SALEN
(PROBLEMAS RESUELTOS DE BIOFÍSICA DEL CBC)
FLUIDOS
|
|

|
| |
|
56b - La composición del aire a nivel del mar, en gramos/litro, es la siguiente:
nitrógeno:
0,975; oxígeno: 0,300; argón: 0,0167; CO2: 5,89 x 10-4. |
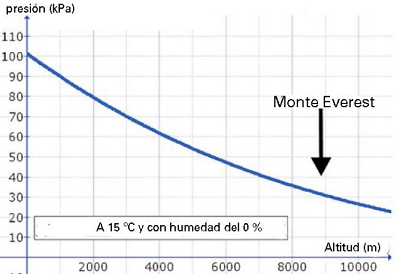
| La presión atmosférica disminuye con la altura. En el siguiente gráfico se muestra la relación entre la presión atmosférica y la altura. Observe que no es una relación lineal ya que la densidad y la gravedad no son constantes con la altura. |
 |
|
|
i) Observando el gráfico, indique cuánto vale aproximadamente la presión atmosférica a nivel del mar, a 4165 m s. n. m. (Olaroz Chico, en provincia de Jujuy, Argentina) y a 8848 m s. n. m. (cima del monte Everest, en la cordillera del Himalaya, Asia).
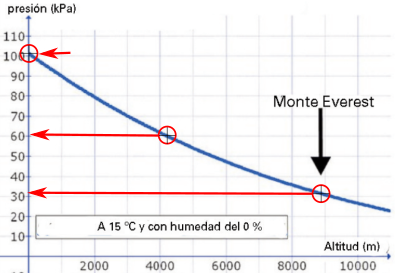
Es muy sencillo, simplemente tenés que saber leer el gráfico. Las alturas de cada localidad las leés en el eje horizontal (abscisas), subís por una vertical hasta intersectar la gráfica, y luego te desplazás por una horizontal hasta el eje vertical (ordenadas) donde aparece la presión atmosférica de cada lugar.
|
|
|
 |
|
|
| Con lo que, aproximadamente, tenemos: |
|
|
A nivel del mar pratm = 101,3 kPa
En olaroz Chico pratm= 61 kPa
Cima del Everest pratm = 32 kPa |
|
|
|
ii) Teniendo en cuenta que la concentración del oxígeno (21%) en aire atmosférico se mantiene constante en los primeros 100 km s. n. m., calcule cuánto vale la presión parcial de oxígeno, en kPa, en los lugares indicados en el ítem anterior.
Como el porcentaje es constante, la presión parciel en cada localidad la hallás secillamente multiplicando cada presión total por 0,21.
|
|
|
A nivel del mar prO2 = 21,27 kPa
En olaroz Chico prO2 = 12,8 kPa
Cima del Everest prO2 = 6,7 kPa |
|
|
|
iii) Sabiendo que a nivel del mar, en un litro de aire atmosférico hay 0,3 gramos de oxígeno, calcule cuántos gramos de oxígeno hay en un litro de aire atmosférico en Olaroz Chico y en la cima del monte Everest.
Al reducirse la presión parcial de oxígeno se reduce también la fracción molar y, lógicamente, la masa. Con simples reglas de tres, podemos hallar las masas para las presiones parciales en las alturas: |
|
|
A nivel del mar mO2 /L = 0,3 g
En olaroz Chico mO2 /L = 0,8 g
Cima del Everest mO2 /L = 0,095 g |
|
|
|
iv) Cuando se asciende, aparecen los efectos del “mal de altura” o “apunamiento”: cansancio extremo, mareos, dolor de cabeza, taquicardia, náuseas, e incluso edema pulmonar en los casos más graves. Justifique sus causas. ¿Por qué se aumenta la frecuencia respiratoria?
En la altura con respirar más rápido (hiperventilación) lograríamos meter en los pulmones la misma cantidad de oxígeno con que los llenamos a nivel del mar. Pero con eso no alcanza debido a que el oxígeno que llega a los alvéolos pulmonares lo hace a una presión menor que la normal (hipoxia alveolar), con lo que se dificulta su incorporación a la hemoglobina de los glóbulos rojos que lo están esperando. Por eso, aunque aumentemos la frecuencia respiratoria, más allá del esfuerzo, gasto energético y cansancio que ello implica, aún así faltará oxígeno en los tejidos de todo el cuerpo.
Los ascensos lentos (semanas o meses) le permiten al organismo ir ajustando la captación de oxígeno, que se logra fundamentalmente aumentando la concentración de glóbulos rojos en la sangre (hematocrito) y de hemoglobina, la molécula transportadora. |
|
|
| |
|
|
DESAFÍO: ¿El tanque de oxígeno en los ascensos, es una solución de urgencia? |
|

|
| |
|
| Algunos derechos reservados.
Se permite su reproducción citando la fuente. Última actualización jul-22. Buenos Aires, Argentina. |
|
|
| | |
|
|

![]()
![]()
![]()
