 |
NO ME SALEN
(APUNTES TEÓRICOS Y EJERCICIOS DE BIOFÍSICA DEL CBC)
CALOR Y TERMODINÁMICA
|
|

|
 |
 |
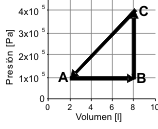
Adicional No me salen 24* - Un mol de gas ideal monoatómico realiza el ciclo ABCA de la figura:
a) Calcular el trabajo, el calor intercambiado y la variación de energía interna para cada tramo del ciclo y para el ciclo entero.
(R = 8,314 J/mol K = 0,082 l atm/mol K;
cp = 5R/2; cV = 3R/2)
|
 |
|
|
| |
Es un ejercicio bastante sencillo, prestá atención.
En casi todos los ejercicios de evoluciones gaseosas suelo hacer un cuadro para ir volcando la información, ya que permite comprender fácilmente los pasos que vamos realizando y chequear que los números van cerrando. |
|
|
De modo que todo lo que voy calculando lo vuelco en la tabla. Por ejemplo, el trabajo de la transformación BC (isocórica) vale cero, ya que no hay variación de volumen.
La variación de energía interna del ciclo vale cero (ya que la energía interna es una función de estado, y en un ciclo se parte y se llega al mismo estado). |
| (J) |
Q |
ΔU |
W |
| AB |
|
|
|
| BC |
|
|
0 |
| CA |
|
|
|
| ciclo |
|
0 |
|
|
|
|
|
Los trabajos de los tramos AB y CA también son sencillos de calcular, ya que podemos calcular las áreas que los representan. |
|
|
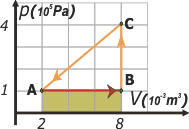 |
El trabajo en la transformación AB (una isobárica) podés calcularlo como
WAB = PAB . ΔVAB
WAB = 1 x 105 Pa . 6 x 10-3 m3
WAB = 600 J
|
|
|
1 litro
es igual a
10-3 m3
|
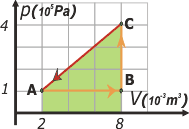
| El trabajo del gas en la transformación CA está representado por el área de un trapecio, o si querés, por la suma de un rectángulo (que ya sabemos cuánto vale) más un triángulo. |
|
|
|
WCA = 600 J + ½ base . altura
WCA = 600 J + ½ 6 x 10-3 m3 . 3 x 105 Pa
WCA = 1.500 J . (–1)
Se trata de un trabajo negativo ya que se corresponde con una reducción de volumen. |
|
|
|
El trabajo del gas durante el ciclo es la suma de los trabajos parciales. De modo que ya tenemos otra respuesta:
Wciclo = – 900 J
Dentro de cada renglón también hay una lógica, que está dada por: |
|
|
Q = ΔU + W
el primer principio de la termodinámica; de modo que el calor intercambiado durante el ciclo debe valer lo mismo que el trabajo, ya que la variación de energía vale cero. |
| (J) |
Q |
ΔU |
W |
| AB |
|
|
600 J |
| BC |
|
|
0 |
| CA |
|
|
–1.500 J |
| ciclo |
–900 J |
0 |
–900 J |
|
|
|
tené en cuenta que redondeé a lo bestia. |
Hasta acá fue demasiado sencillo. Lo que viene no es tan difícil. Las variaciones de energía interna de cualquier transformación en la que haya cambios de temperatura se calcula de la siguiente manera:
ΔU = cv n ΔT
De modo que necesitamos conocer las temperaturas en cada estado para conocer las diferencias de temperatura en cada transformación y calcular las variaciones de energía interna. Esas temperaturas no son dato, pero utilizando la ecuación de estado de los gases ideales (justamente para poder hacer esto es que el enunciado nos aclara que de un gas ideal se trata)...
TA = PA VA / n R = 24 K
TB = PB VB / n R = 96 K
TC = PC VC / n R = 385 K |
|
Ecuación de estado de los gases ideales:
P V = n R T |
|
Ahora sí, calculamos...
ΔUAB = cv n ΔTAB = 900 J
ΔUBC = cv n ΔTBC = 3.600 J
ΔUCA = cv n ΔTCA = – 4.500 J |
| (J) |
Q |
ΔU |
W |
| AB |
|
900 J |
600 J |
| BC |
|
3.600 J |
0 |
| CA |
|
– 4.500 J |
–1.500 J |
| ciclo |
–900 J |
0 |
–900 J |
|
|
|
calor negativo significa que el gas lo pierde
trabajo negativo significa que el gas lo recibe |
Para conocer los calores intercambiados en cada tramo ya no tenemos que hacer muchas cuentas... aplicando el primer principio o sea, completando las sumas de cada renglón) podemos obtenerlos fácilmente.
Pero si te queda alguna duda podés, al menos, resolver los tramos AB y BC que transcurren a presión constante y a volumen constante respectivamente.
QAB = cp n ΔTAB = 2,5 . 8,314 J/molK . 1 mol . 72 K = 1.500 J
QBC = cv n ΔTBC = 1,5 . 8,314 J/molK . 1 mol . 289 K = 3.600 J
|
|
|
Lo único que falta el el calor del tramo CA, que lo obtenemos haciendo las sumas horizontales (primer principio), y las verticales (completar el ciclo).
Y ya tenemos todo calculado. Antes de pasar a otro ejercicio revisá una vez más que todas las sumas horizontales y verticales nos hayan dado correctamente. Si así no fuera... o yo me equivoqué, o se equivocó Lord Kelvin. |
| (J) |
Q |
ΔU |
W |
| AB |
1.500 J |
900 J |
600 J |
| BC |
3.600 J |
3.600 J |
0 |
| CA |
–6.000 J |
– 4.500 J |
–1.500 J |
| ciclo |
–900 J |
0 |
–900 J |
|
|
|
|
Tenés otro ejercicio muy parecido acá. |
|
|
| |
 |
| *Este ejercicio fue parte del examen, 2do. parcial, tomado el 26-jun-12. |
|
|
| Desafío: ¿Cuánto valdrá la variación de entropía para todo el ciclo? |
|
| |
|
| Algunos derechos reservados.
Se permite su reproducción citando la fuente. Agradezco a Ignacio Bosio y a Eduardo Flores por el envío de sendas erratas. Última actualización jul-12. Buenos Aires, Argentina. |
|
|
| | |
|
|

